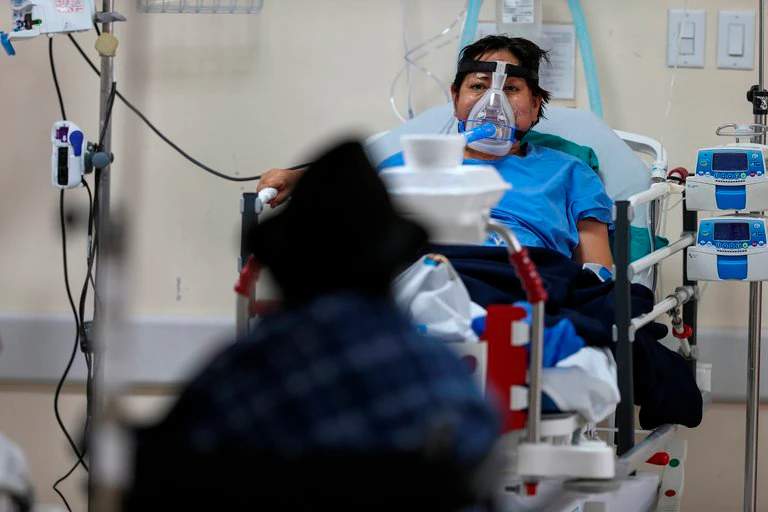
El fármaco autorizado en Estados Unidos es para personas con factores de riesgo de desarrollar cuadros graves que requieren internación en el hospital. La evidencia preliminar demuestra que el fármaco previene la progresión de la enfermedad al evitar que el virus afecte a más células sanas en el organismo.
La agencia regulatoria de medicamentos en los Estados Unidos, más conocida por su sigla en inglés como la FDA, autorizó para uso de emergencia un nuevo medicamento para prevenir que los adolescentes y los adultos con factores de riesgo desarrollen cuadros severos y pierdan la vida si se contagian el coronavirus.
El medicamento lleva el nombre genérico de “sotrovimab” y fue autorizado solo para indicar en pacientes leves y moderados que aún no hayan requerido hospitalización ni estén usando respirador.
Según la especificación técnica de su aprobación, se trata de un anticuerpo monoclonal en investigación de doble acción frente al SARS-CoV-2. Los datos preclínicos sugieren que tiene el potencial de bloquear la entrada del virus en las células sanas y que puede tener una mayor capacidad para eliminar las células infectadas.
Días atrás, también el Comité de Medicamentos para Uso Humano de la Agencia Europea de Medicamentos (EMA) había emitido una opinión positiva de sotrovimab después de revisar los datos del ensayo clínico en fase 3 que aún está en curso.
El nuevo tratamiento es el resultado de un trabajo en colaboración entre investigadores científicos de la empresa farmacéutica GSK con Vir Biotechnology, una compañía de inmunología que combina sus conocimientos inmunológicos con tecnologías de vanguardia para tratar y prevenir enfermedades infecciosas grave. Pertenece al grupo de los anticuerpos monoclonales, que empezaron a desarrollarse para diferentes enfermedades a partir de los trabajos pioneros del científico argentino César Milstein y el alemán Georges Köhler en 1975, quienes ganaron luego el Premio Nobel de Medicina.
“Este nuevo fármaco, el sotrovimab, es un anticuerpo monoclonal más específico a diferencia de otros medicamentos que ya fueron autorizados por la agencia regulatoria estadounidense para la misma etapa de la enfermedad”, dijo a Infobae la doctora Isabel Cassetti, directora médica de Helios Salud y miembro de la Sociedad Argentina de Infectología. Los otros anticuerpos autorizados se usan en combinación con otros. En cambio, el nuevo fármaco autorizado se dirige a la proteína Spike del coronavirus: impide la entrada del virus en las células y no requiere de combinación con otros. Se indica en una sola dosis en pacientes ambulatorios que tienen factores de riesgo de progresión, señaló la especialista.
El anticuerpo monoclonal sotromibab está indicado solo para el tratamiento durante los primeros 10 días de la infección después del inicio de los síntomas y confirmada por un testeo.
La agencia regulatoria de Estados Unidos autorizó al sotrovimab para el tratamiento del COVID-19 de leve a moderado en adultos y pacientes pediátricos (de 12 años en adelante que pesen al menos 40 kilogramos) con un hisopado positivo y que tengan un alto riesgo de progresión al COVID-19 grave, incluyendo la hospitalización o la muerte.
“El anticuerpo puede indicarse en pacientes ambulatorios que, antes de contagiarse coronavirus, tenían hipertensión, enfermedades cardiovasculares o respiratorias, insuficiencia renal, inmunosuprimidos, enfermedades oncológicas, entre otros factores de riesgo”, comentó la doctora Cassetti.
Se puede administrar durante los primeros diez días de la infección por el coronavirus a partir del inicio de los síntomas o del resultado positivo de la PCR. Como también ocurre con los otros anticuerpos monoclonales, no se puede indicar cuando el paciente con COVID-19 ya necesitó de la asistencia con respirador como oxigenoterapia. “El sotrovimab es para una estrategia inicial de tratamiento para COVID-19”, precisó Cassetti.
De acuerdo con la FDA de Estados Unidos, la terapia con sotrovimab resulta también eficaz cuando una persona con factores de riesgo se contagia con una de las variantes de preocupación del coronavirus /OPS
También, otro beneficio del anticuerpo monoclonal sotrovimab es su perfil: “Es activo frente a las diferentes variantes de preocupación que se han detectado. Por esto, sería un gran aporte para que los pacientes con factores de riesgo que adquieran la infección por el coronavirus reduzcan el riesgo de internación y muerte”, opinó Cassetti.
La doctora Adrienne Shapiro, M.D., Ph.D., especialista en enfermedades infecciosas del Fred Hutchinson Cancer Research Center e investigadora del estudio clínico COMET-ICE que midió la efectividad de la droga, afirmó: “Los anticuerpos monoclonales como sotrovimab pueden ser una de nuestras herramientas más efectivas para combatir el COVID-19. Si bien las medidas preventivas, incluidas las vacunas, pueden reducir el número total de casos, sotrovimab es una opción de tratamiento importante para quienes contraen COVID-19 y se consideran pacientes de alto riesgo, ya que les evita llegar a la hospitalización o a un desenlace peor.”
“Nuestro enfoque científico distintivo nos ha llevado a un solo anticuerpo monoclonal que, sobre la base de un análisis interino, logró una reducción del 85% de las hospitalizaciones o las muertes por todas las causas e, in vitro, ha demostrado que conserva su actividad contra todas las variantes preocupantes conocidas, incluida la variante emergente de la India. Creo que sotrovimab es una nueva opción de tratamiento fundamental en la lucha contra la pandemia actual y también podría serlo para futuros brotes de coronavirus. El objetivo de Vir no solo es ofrecer una terapia clínicamente efectiva contra el COVID-19, sino también brindar un tratamiento efectivo contra las variantes del SARS-CoV-2 y las posibles pandemias del futuro”, agregó el especialista y CEO de Vir, George Scangos.
De acuerdo con el comunicado de la FDA, la seguridad y la eficacia de la terapia con sotrovimab sigue siendo evaluada para el tratamiento de la COVID-19. Se aclaró que “no está autorizada para pacientes que estén hospitalizados por COVID-19 o que requieran oxigenoterapia”. No ha demostrado ser beneficioso en pacientes hospitalizados con COVID-19. “Los anticuerpos monoclonales pueden asociarse con peores resultados clínicos cuando se administran a pacientes hospitalizados que requieren oxígeno de alto flujo o ventilación mecánica”, expresó la FDA.
“Con la autorización de este tratamiento con anticuerpos monoclonales, estamos proporcionando otra opción para ayudar a mantener a los pacientes de alto riesgo con COVID-19 fuera del hospital”, dijo la doctora Patrizia Cavazzoni, directora del Centro de Evaluación e Investigación de Medicamentos de la FDA. “Es importante ampliar el arsenal de terapias con anticuerpos monoclonales que se espera que mantengan la actividad contra las variantes circulantes de COVID-19 en los Estados Unidos”.
Ya hay 12 vacunas autorizadas en el mundo. Pero no toda la población accede Mientras tanto, hay gente que se siguen infectando con el coronavirus. El nuevo anticuerpo monoclonal autorizado en EEUU se suma para dar respuesta a la etapa inicial de la enfermedad.
Los anticuerpos monoclonales son proteínas fabricadas en el laboratorio que imitan la capacidad del sistema inmune para controlar antígenos dañinos como los virus. En el caso del sotrovimab es un anticuerpo que fue diseñado para bloquear la adhesión y la entrada del virus en las células humanas.
La agencia regulatoria consideró que cuando el sotrovimab se utiliza para tratar solo a la población autorizada (adolescentes y adultos -incluyendo adultos mayores- con factores de riesgo previos), “los beneficios conocidos y potenciales superan los riesgos conocidos y potenciales del medicamento. No hay tratamientos adecuados, aprobados y disponibles como alternativa a sotrovimab”, advirtió.
Consultado por Infobae, Ventura Simonovich, vicepresidente de la Asociación Argentina de Farmacología Experimental y jefe de Farmacología Clínica del Hospital Italiano de Buenos Aires, consideró: “El desarrollo del sotrovimab para pacientes con factores de riesgo es alentador, pero que necesitamos saber más sobre los resultados del ensayo clínico cuando se publiquen”.
Los datos que respaldan la autorización de la FDA se basan en un análisis provisional de un ensayo clínico aleatorizado, doble ciego y controlado con placebo en 583 adultos no hospitalizados con síntomas de COVID-19 de leves a moderados y un resultado positivo en la prueba del SARS-CoV-2. De estos pacientes, 291 recibieron sotrovimab y 292 recibieron placebo en los cinco días siguientes a la aparición de los síntomas de COVID-19.
Para autorizar el anticuerpo monoclonal, la FDA se basó en el ensayo clínico en marcha. La hospitalización o la muerte se produjeron en 21 (7%) pacientes que recibieron placebo en comparación con 3 (1%) pacientes tratados con sotrovimab, una reducción del 85%. Como posibles efectos secundarios del sotrovimab, se incluyen reacciones alérgicas, erupción cutánea y diarrea, entre otros.
El doctor Hal Barron, Gerente Científico y Presidente de Investigación y Desarrollo de GSK, concluyó lo siguiente: “Si bien la rapidez con la que se está llevando a cabo la vacunación contra COVID-19 en los EEUU es alentadora, a pesar de este gran esfuerzo, aún existe la necesidad de ayudar a prevenir que los pacientes infectados desarrollen complicaciones. Luego de poco más de un año desde que comenzamos nuestra colaboración y menos de 10 meses desde que comenzamos los estudios clínicos, nos alegra enormemente que, a partir de hoy, los beneficios de este peculiar anticuerpo monoclonal ahora estén disponibles para los pacientes que lo necesitan”.
Sotrovimab continúa evaluándose en los estudios clínicos que se encuentran en curso. Ya en el primer semestre de 2021, está previsto efectuar un análisis de los datos de seguridad y eficacia el Día 29 en la población completa del estudio COMET-ICE. En el segundo semestre de 2021, GSK y Vir tienen planificado enviar a la FDA una Solicitud de Licencia para Productos Biológicos.
El criterio de valoración principal fue la progresión de la enfermedad, que es definida como la hospitalización durante más de 24 horas para el tratamiento agudo de cualquier enfermedad o la muerte por cualquier causa hasta el día 29. La hospitalización o la muerte se produjeron en 21 (7%) pacientes que recibieron placebo en comparación con 3 (1%) pacientes tratados con sotrovimab, una reducción del 85%. Como posibles efectos secundarios del sotrovimab, se incluyen reacciones alérgicas, erupción cutánea y diarrea, entre otros.
También se tuvo en cuenta que las pruebas de laboratorio demostraron que el sotrovimab es eficaz aun cuando las personas con factores de riesgo han sido infectadas con las variantes de preocupación. Hasta ahora el fármaco no ha recibido aprobación o autorización en algún país de América Latina.
“Todas las estrategias de tratamiento que se van desarrollando para COVID-19 y que demuestran beneficios deben ser indicadas en el momento adecuado de la enfermedad”, comentó la doctora Cassetti. “En el caso de los anticuerpos monoclonales, su utilidad se da al principio. En el caso de los corticoides, se indica cuando el paciente se encuentra en estado crítico y requiere oxígeno. Hay que considerar bien la etapa de la enfermedad que atraviesa cada paciente para indicar el tratamiento adecuado”.
Fuente: INFOBAE